Bu çalışma materyali, "Periyodik Sistem" konusunu AYT (Yükseköğretim Kurumları Sınavı) Kimya müfredatına uygun olarak, bir ders kaydından derlenerek hazırlanmıştır.
📚 Periyodik Sistem: AYT Kimya İçin Kapsamlı Çalışma Rehberi
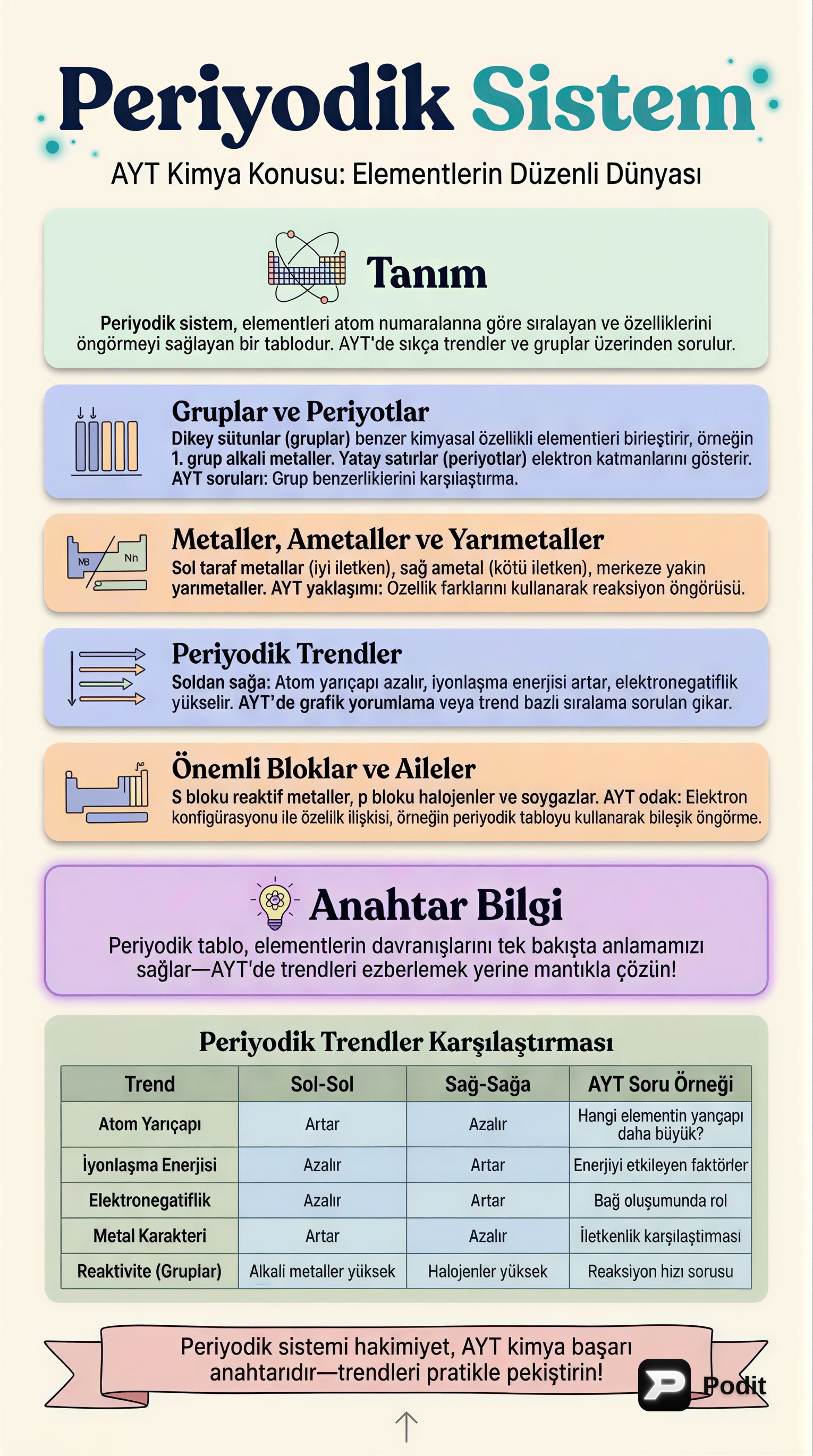
Giriş: Periyodik Sisteme Genel Bakış
Periyodik sistem, kimya biliminin temel taşlarından biridir ve elementlerin atom numaralarına ve benzer kimyasal özelliklerine göre düzenlendiği bir tablodur. ✅ Bu sistem, elementlerin davranışlarını, reaksiyonlarını ve fiziksel özelliklerini anlamak için kritik bir araçtır. Özellikle AYT Kimya sınavında, periyodik sistem ve periyodik özellikler konuları önemli bir yer tutar. Bu rehber, periyodik sistemin temel yapısını, elementlerin sınıflandırılmasını ve bu bilgilerin AYT'deki önemini detaylı bir şekilde ele almaktadır.
Periyodik Sistemin Yapısı ve Elementlerin Sınıflandırılması
Periyodik sistem, elementlerin düzenli bir şekilde sıralandığı bir yapıdır.
1️⃣ Periyotlar ve Gruplar
- Periyotlar: Yatay sıralardır. Toplam yedi periyot bulunur. Bir elementin periyot numarası, en dış katmanındaki elektronların bulunduğu enerji seviyesini (kabuk sayısını) gösterir.
- Gruplar: Dikey sütunlardır. Toplam on sekiz grup bulunur. Grup numarası genellikle değerlik elektron sayısı ve dolayısıyla elementin kimyasal reaktivitesi hakkında bilgi verir.
2️⃣ Ana Grup (A) ve Geçiş Metali (B) Grupları
- A Grupları (Ana Grup Elementleri): 1A'dan 8A'ya kadar olan gruplardır. Bu elementlerin değerlik elektronları s veya p orbitallerinde bulunur.
- B Grupları (Geçiş Metalleri): 3B'den 2B'ye kadar olan gruplardır. Bu elementlerin değerlik elektronları d orbitallerinde bulunur.
- İç Geçiş Metalleri: Lantanitler ve Aktinitler olarak bilinen, periyodik tablonun altında ayrı olarak gösterilen f bloğu elementleridir.
3️⃣ Bloklara Göre Sınıflandırma
Elementler, son elektronlarının yerleştiği orbital türüne göre dört ana bloğa ayrılır:
- s bloğu: 1A ve 2A gruplarını içerir. (Örn: Na, Mg)
- p bloğu: 3A'dan 8A'ya kadar olan grupları içerir. (Örn: Al, O, Ne)
- d bloğu: Geçiş metallerini içerir. (Örn: Fe, Cu)
- f bloğu: İç geçiş metallerini (lantanitler ve aktinitler) içerir.
4️⃣ Özel Gruplar ve Özellikleri
AYT için bazı özel grupların özellikleri detaylıca bilinmelidir:
- 1A Grubu (Alkali Metaller): Lityum (Li), Sodyum (Na), Potasyum (K) gibi elementler. Çok reaktiftirler, bileşiklerinde +1 değerlik alırlar.
- 2A Grubu (Toprak Alkali Metaller): Berilyum (Be), Magnezyum (Mg), Kalsiyum (Ca) gibi elementler. Alkali metallere göre daha az reaktiftirler, bileşiklerinde +2 değerlik alırlar.
- 7A Grubu (Halojenler): Flor (F), Klor (Cl), Brom (Br), İyot (I) gibi elementler. Çok reaktiftirler, bileşiklerinde genellikle -1 değerlik alırlar.
- 8A Grubu (Soy Gazlar): Helyum (He), Neon (Ne), Argon (Ar) gibi elementler. Kararlı yapıya sahiptirler, genellikle kimyasal tepkimeye girmezler.
Periyodik Özellikler ve Eğilimler
Periyodik sistemde elementlerin bazı özellikleri düzenli eğilimler gösterir. Bu eğilimleri bilmek, elementlerin davranışlarını tahmin etmede anahtardır.
1️⃣ Atom Yarıçapı
📚 Tanım: Bir atomun çekirdeği ile en dıştaki elektron kabuğu arasındaki mesafedir.
- Periyotta (soldan sağa): Genellikle azalır. (Çekirdek yükü artar, elektronlar daha güçlü çekilir.)
- Grupta (yukarıdan aşağıya): Artar. (Kabuk sayısı artar.)
2️⃣ İyonlaşma Enerjisi (İE)
📚 Tanım: Gaz halindeki nötr bir atomdan bir elektron koparmak için gereken minimum enerjidir.
- Periyotta (soldan sağa): Genellikle artar. (Atom yarıçapı küçülür, elektronu koparmak zorlaşır.)
- Grupta (yukarıdan aşağıya): Azalır. (Atom yarıçapı büyür, elektronu koparmak kolaylaşır.)
- ⚠️ İstisnalar:
- 2A > 3A (Örn: Be > B)
- 5A > 6A (Örn: N > O) Bu istisnalar, tam dolu veya yarı dolu orbitallerin küresel simetrik ve daha kararlı yapısından kaynaklanır.
3️⃣ Elektron İlgisi
📚 Tanım: Gaz halindeki nötr bir atomun bir elektron alması sırasındaki enerji değişimidir. Genellikle ekzotermiktir (enerji açığa çıkar).
- Periyotta (soldan sağa): Genellikle artar (daha negatif değer alır).
- Grupta (yukarıdan aşağıya): Genellikle azalır (daha az negatif değer alır).
- En yüksek elektron ilgisi: Klor (Cl) atomundadır.
4️⃣ Elektronegatiflik
📚 Tanım: Bir atomun kimyasal bağdaki elektronları kendine çekme yeteneğidir.
- Periyotta (soldan sağa): Artar.
- Grupta (yukarıdan aşağıya): Azalır.
- En elektronegatif element: Flor (F).
5️⃣ Metalik ve Ametalik Özellikler
- Metalik Özellik: Elektron verme eğilimi ile ilişkilidir.
- Periyotta (soldan sağa): Azalır.
- Grupta (yukarıdan aşağıya): Artar.
- Ametalik Özellik: Elektron alma eğilimi ile ilişkilidir.
- Periyotta (soldan sağa): Artar.
- Grupta (yukarıdan aşağıya): Azalır.
AYT Soru Yaklaşımları ve Önemli Noktalar
AYT Kimya'da periyodik sistemle ilgili sorular genellikle aşağıdaki becerileri ölçer:
- Elementlerin Konumundan Özellik Karşılaştırma: Verilen elementlerin periyodik tablodaki konumlarından yola çıkarak atom yarıçapı, iyonlaşma enerjisi, elektronegatiflik gibi özelliklerini sıralama.
- 💡 Örnek: Na, Mg, Al elementlerinin atom yarıçaplarını karşılaştırın. (Na > Mg > Al çünkü aynı periyotta soldan sağa azalır.)
- Elektron Dizilimi ile Periyodik Konum İlişkisi: Bir elementin elektron diziliminden periyodik tablodaki yerini (periyot ve grup numarasını) belirleme.
- 💡 Örnek: [Ne] 3s² 3p³ elektron dizilimine sahip elementin periyodik tablodaki yerini bulun. (3. periyot, 5A grubu)
- Periyodik Özelliklerdeki Eğilimleri Yorumlama: Genel eğilimlerin yanı sıra, iyonlaşma enerjisi istisnaları gibi özel durumları açıklama.
- ⚠️ Unutmayın: 2A-3A ve 5A-6A istisnaları AYT'de sıkça sorulur.
- Özel Grupların Özellikleri: 1A, 2A, 7A ve 8A gruplarının genel özellikleri, bileşik oluşturma eğilimleri ve fiziksel halleri gibi bilgiler önemlidir.
Sonuç
Periyodik sistem, kimya biliminin temelini oluşturan ve AYT Kimya sınavında başarılı olmak için mutlak suretle hakim olunması gereken bir konudur. Elementlerin periyodik tablodaki konumlarını, grup ve periyot özelliklerini, ayrıca atom yarıçapı, iyonlaşma enerjisi, elektron ilgisi ve elektronegatiflik gibi periyodik özelliklerdeki eğilimleri ve istisnaları derinlemesine anlamak, sınavda karşılaşılabilecek çeşitli soru tiplerini doğru bir şekilde çözmek için kritik bir beceridir. Bu bilgilerin sağlam bir şekilde öğrenilmesi, kimyanın diğer konularını anlamak için de güçlü bir temel oluşturacaktır. 📈