Kaynak Bilgisi: Bu çalışma materyali, ders notları, PDF/PowerPoint metinleri ve sesli ders kaydından derlenmiştir.
DNA: Genetik Materyal, Mutasyonlar ve Tamir Mekanizmaları 🧬
Giriş
Deoksiribonükleik asit (DNA), canlıların genetik bilgisini taşıyan, kopyalayan ve ifade eden temel bir moleküldür. Yaşamsal fonksiyonların merkezinde yer alan DNA, aynı zamanda tür içi çeşitliliğin ve evrimin ana itici güçlerinden biri olan mutasyonlara da ev sahipliği yapar. Bu çalışma materyali, DNA'nın genetik materyal olarak özelliklerini, mutasyonların tanımını, sınıflandırılmasını, oluşum nedenlerini ve hücrelerin bu değişiklikleri nasıl onardığını detaylı bir şekilde incelemektedir.
Genetik Materyal Olarak DNA'nın Temel Özellikleri ✅
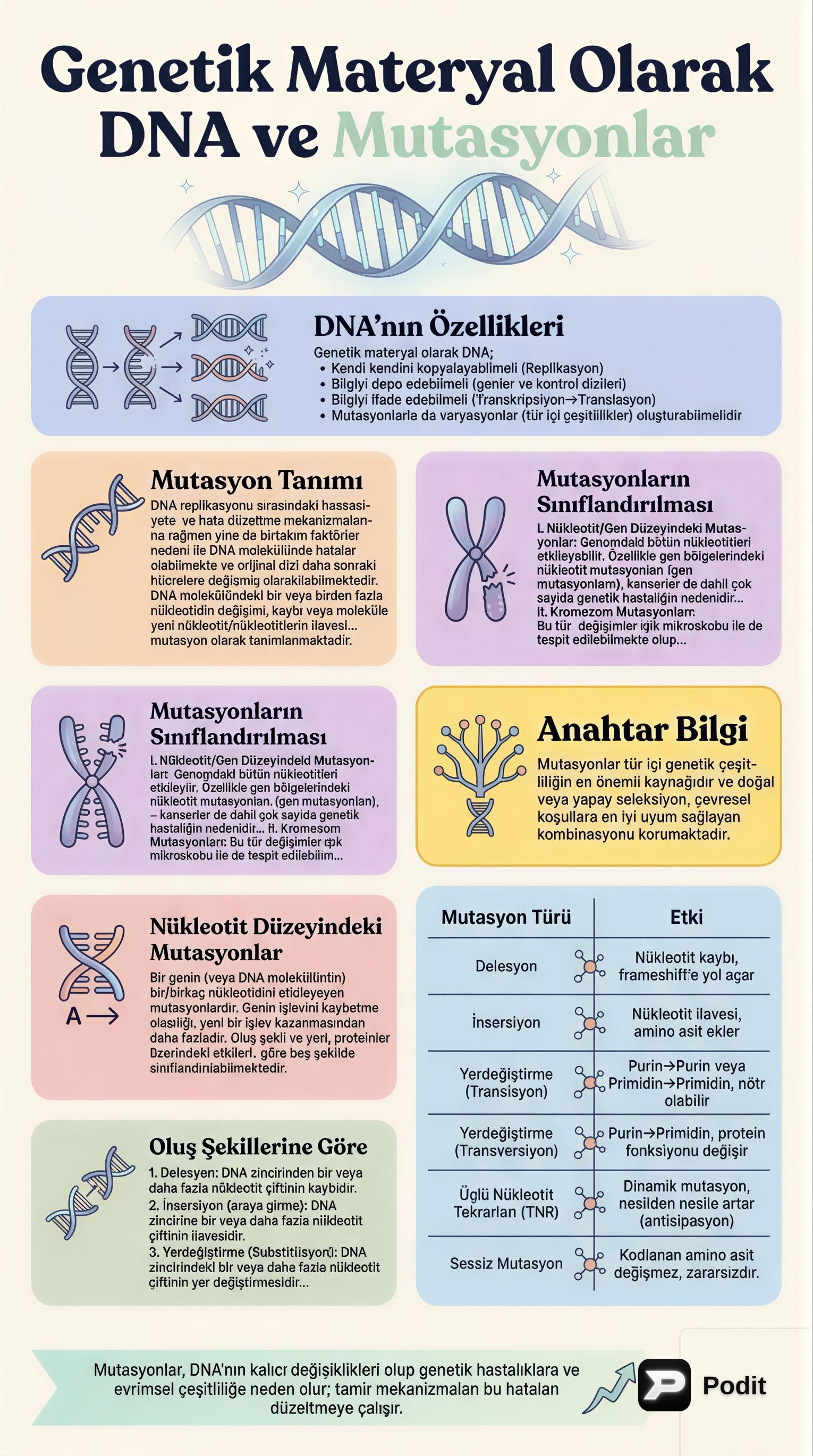
DNA'nın genetik materyal olarak kabul edilebilmesi için belirli kriterleri karşılaması gerekir:
- Kendi Kendini Kopyalayabilme (Replikasyon): 🔄 Genetik bilginin nesilden nesile aktarılabilmesi için DNA'nın doğru ve eksiksiz bir şekilde kopyalanabilmesi esastır.
- Bilgiyi Depolayabilme: 📚 Genler ve kontrol dizileri aracılığıyla tüm hücresel fonksiyonlar için gerekli bilgiyi güvenli bir şekilde saklayabilmelidir.
- Bilgiyi İfade Edebilme (Transkripsiyon → Translasyon): 🗣️ Depolanan bilginin proteinlere dönüştürülerek hücresel işlevlerde kullanılabilmesi gerekir.
- Mutasyonlarla Varyasyon Oluşturabilme: 📈 Tür içi çeşitliliğin ve evrimin temelini oluşturan kalıcı değişiklikler (mutasyonlar) yapabilme yeteneğine sahip olmalıdır.
Mutasyon Nedir? 📚
Mutasyon, DNA replikasyonu sırasındaki hassasiyete ve hata düzeltme mekanizmalarına rağmen, DNA molekülünde meydana gelen kalıcı değişikliklerdir. Bu değişiklikler şunları içerebilir:
- Bir veya birden fazla nükleotidin değişimi, kaybı veya ilavesi.
- Gen ifadesinde değişikliğe neden olan yeni düzenlenmeler (DNA rearrangements).
- Kromozomların sayı ve yapısındaki değişiklikler (büyük çapta yeniden düzenlenmeler).
Bu kalıcı değişiklikler, genetik hastalıkların ve evrimin temelini oluşturur.
Mutasyonların Sınıflandırılması 📊
Mutasyonlar genel olarak iki ana düzeyde incelenir:
I. Nükleotit/Gen Düzeyindeki Mutasyonlar (Gen/Nokta Mutasyonları)
Bir genin (veya DNA molekülünün) bir veya birkaç nükleotidini etkileyen mutasyonlardır. Genin işlevini kaybetme olasılığı, yeni bir işlev kazanmasından daha fazladır.
a) Oluş Şekillerine Göre:
- Delesyon: DNA zincirinden bir veya daha fazla nükleotit çiftinin kaybıdır.
- İnsersiyon (Araya Girme): DNA zincirine bir veya daha fazla nükleotit çiftinin ilavesidir.
- Üç veya katları kadar nükleotit kaybı/ilavesi (stop kodonlardan biri değilse) proteine amino asit kaybı veya ilavesine neden olur.
- Yerdeğiştirme (Substitüsyon): DNA zincirindeki bir veya daha fazla nükleotit çiftinin yer değiştirmesidir.
- Transisyon: Pürin → Pürin (A ↔ G) veya Pirimidin → Pirimidin (T ↔ C) değişimi.
- Transversiyon: Pürin → Pirimidin (A/G → C/T) veya Pirimidin → Pürin (C/T → A/G) değişimi.
- Üçlü Nükleotit Tekrarları (TNR) / Dinamik Mutasyonlar: Genlerin "sıcak bölgelerinde" üçlü nükleotit dizilerinin farklı sayılarda tekrarları sonucu ortaya çıkar.
- Antisipasyon: Mayoz sırasında tekrar sayısının artma eğiliminde olması ve nesilden nesile artırılarak aktarılmasıdır.
- Örnek Hastalıklar: SCA tipleri, Fragile-X sendromu, Miyotonik Distrofi (MD), Friedreich Ataksisi.
b) Protein Üzerindeki Etkilerine Göre:
- Sessiz (Silent) Mutasyonlar: Nükleotit değişimine rağmen kodlanan amino asit değişmez (örn. Lizin AAA ve AAG ile kodlanır). Genellikle zararsızdır.
- Yanlış Anlamlı (Missense) Mutasyonlar: Nükleotit değişimi kodlanan amino asidi de değiştirir. Protein fonksiyonu değişmiyorsa "nötr" olarak adlandırılır.
- Örnek: Orak Hücre Anemisi'nde Hemoglobin geninin 6. pozisyonundaki glutaminin (Glu) valine (Val) dönüşümü (T→A nokta mutasyonu) eritrositlerin orak şekilli olmasına neden olur.
- Zincir Sonlandırıcı (Nonsense) Mutasyonlar: Nükleotit değişimi o noktada stop kodon oluşturarak protein sentezinin durmasına neden olur.
- Çerçeve Kayması (Frame-Shift) Mutasyonları: Üç ve katları olmayan sayıdaki delesyon/insersiyonlar okuma çerçevesini değiştirir. Sonuçta orijinalinden çok farklı, işlevsiz bir protein sentezlenir.
c) Oluş Yerlerine Göre:
Mutasyonlar genlerin kodlama dizileri dışında da oluşabilir ve gen ekspresyonunu etkileyebilir.
- Ekzon Mutasyonları: Genin kodlanan bölgelerinde oluşur, protein/RNA'nın yapı, fonksiyon ve büyüklüğünü etkiler.
- Promotör Bölgesi Mutasyonları: Transkripsiyon oranını artırarak/azaltarak veya genin normal kontrol mekanizmasını bozarak etki gösterir.
- 5'-UTR/3'-UTR Bölgesi Mutasyonları: mRNA'nın translasyonunu veya stabilitesini değiştirebilir.
- Birleştirme Bölgesi (Splice-Site) Mutasyonları: Splicing olayını etkiler, ekzon kaybına veya intron dizilerinin ekzon olarak kabul edilmesine yol açabilir.
- İntron Mutasyonları: Çoğu etkisizdir, ancak bazıları splicing olayını etkileyerek inaktif veya aktivitesi azalmış proteinlere neden olabilir.
- Genlerarası (Diğer) Bölgelerdeki Mutasyonlar: Yukarıdaki bölgeler dışında herhangi bir yerde oluşan mutasyonlardır.
d) Kalıtım Şekillerine Göre:
- Germ-line Mutasyonlar: Üreme (veya öncü) hücrelerinde oluşur ve bir sonraki kuşağa aktarılır.
- Somatik Mutasyonlar: Üreme hücreleri dışındaki vücut hücrelerinde oluşur ve bir sonraki kuşağa aktarılmaz. Fenotipik etkileri gelişimin evresine bağlıdır (örn. kanserler).
e) Etki Şekillerine Göre:
- Dominant (Baskın) Mutasyon: Mutasyon genin alellerinden sadece birinde oluşsa bile etkisini gösterir (heterozigot mutant).
- Resesif (Çekinik) Mutasyon: Mutasyon genin her iki alelinde de oluştuğunda (homozigot mutant) etkisini gösterir.
II. Kromozom Mutasyonları
Kromozomların sayısal ve yapısal düzensizlikleridir. Işık mikroskobu ile tespit edilebilirler ve genellikle daha büyük çaplı yeniden düzenlenmelerdir.
Mutasyonlarla İlgili Genel Bilgiler 💡
- Çeşitlilik Kaynağı: Mutasyonlar, tür içi genetik çeşitliliğin en önemli kaynağıdır.
- Geri Dönüşümlü (Reverse) Mutasyon: Başka bir mutasyonun mutant aleli tekrar normale döndürmesidir.
- Baskılayıcı (Suppressor) Mutasyon: Bir mutasyonun fenotipik etkisini baskılayan başka bir mutasyondur (intragenik veya intergenik olabilir).
- Koşullu (Conditional) Mutasyon: Fenotipik etkisi belli koşullar (ısı, ışık vb.) altında ortaya çıkan mutasyondur.
- Ölümcül (Lethal) Mutasyon: Canlının ölümüne neden olabilecek allel oluşumuna yol açar.
- Faydalı Mutasyon: Canlının yaşama ve üremesini iyileştirecek bir özellik kazandıran mutasyondur.
Mutasyonların Nedenleri ⚠️
Mutasyonlar kendiliğinden (spontan) veya dış etkenler (indükleyici ajanlar) sonucu oluşabilir.
I. Spontan (Kendiliğinden) Nedenler:
Hücre dışı bir etki olmaksızın, biyolojik süreçlerdeki anormalliklere bağlı olarak DNA'da oluşan değişikliklerdir.
- DNA Replikasyon Hataları: DNA polimerazlar tarafından sentez sırasında oluşan hatalar.
- Zehirli Metabolik Ürünler: Normal metabolik süreçte oluşan reaktif ürünlerin DNA yapısını değiştirmesi.
- Nükleotit Yapısında Spontan Değişiklikler:
- Deaminasyon: Adenin, Sitozin ve Guanin bazlarındaki amin (NH2) grubunun değişmesiyle farklı bazlarla eşleşme potansiyeli kazanmaları (örn. Sitozinin deaminasyonu ile Urasil oluşumu).
- Depürinasyon: Pürin bazlarının (A/G) kaybı sonucu apürinik bölgelerin oluşması. Replikasyon sırasında bu bölgelerin karşısına rastgele nükleotitler gelebilir.
- Tautomerik Kaymalar (Tautomeric Shifts): Bazlardaki hidrojen atomlarının pozisyon değiştirmesiyle daha az kararlı formlara dönüşmeleri ve yanlış baz eşleşmelerine neden olmaları.
- Kromozomların Sayı ve Yapısını Değiştiren Olaylar: Anormal rekombinasyon veya anormal kromozom ayrılması.
- Transpozonlar: Hücre içi anormal durumlar transpozon hareketliliğine neden olarak genomik kararsızlığa yol açabilir.
II. İndükleyici Ajanlar (Mutajenler) Etkisiyle:
Mutasyona neden olan herhangi bir ajana mutajen denir. Mutajenler üç gruba ayrılır:
A. Kimyasal Mutajenler:
- Baz Analogları: Nükleik asit biyosentezi sırasında pürin ve pirimidinler yerine geçebilen moleküllerdir (örn. 5-Bromourasil). Tautomerik kayma olasılığını artırarak mutasyona neden olurlar.
- Alkilleyici Ajanlar: DNA bazlarına alkil (metil/etil) grubu ekleyerek baz eşleşme eğilimlerini değiştirirler (örn. Nitrojen mustard, EMS).
- İnterkalasyon Ajanları: DNA'nın bazları arasına sıkışarak çift sarmallı yapıyı esnemez hale getirir ve çerçeve kayması mutasyonlarına neden olurlar (örn. Etidyum Bromür, Akridin boyaları).
- Aflatoksin B1 (AFB1): Guanine tutunarak apürinik bölgeler oluşturur ve güçlü bir karsinojendir.
B. Fiziksel Mutajenler:
- İyonize Radyasyon (X ışını, Gama ışını, Kozmik ışın): Yüksek enerjilidir, DNA'da kırıklara, serbest radikal oluşumuna ve nokta mutasyonlarına neden olur.
- Noniyonize Radyasyon (Ultraviyole (UV) ışınları): Pirimidin bazları tarafından emilir ve pirimidin dimerleri (örn. timin dimerleri) oluşturarak DNA replikasyonunu bloke edebilir.
C. Biyolojik Mutajenler:
- Virüsler: Genomlarını enfekte ettikleri hücre genomuna rastgele yerleştirerek mutasyonlara neden olabilirler.
- Bakteriler: Bazı bakteriler (örn. Helicobacter pylori) mutajenik etki gösterebilir.
💡 Ames Testi: Kimyasalların mutajenik potansiyelini hızlı ve pratik bir şekilde belirlemek için kullanılan bir yöntemdir. Histidin sentezleyemeyen Salmonella suşları kullanılarak geri mutasyon oranları ölçülür.
DNA Tamir Mekanizmaları 🛠️
Mutasyonların çoğu zararlı olduğundan, DNA tamir mekanizmaları canlıların hayatta kalabilmesi için son derece önemlidir. Bu mekanizmalar, genomik bütünlüğün korunmasında hayati bir rol oynar.
Genel olarak tamir mekanizmaları şu adımları izler:
- DNA ipliğini tarar ve düzensizlikleri tespit eder.
- Hasarlı nükleotitler çıkartılır.
- Replikasyon enzimleri tarafından doğrusu sentezlenir.
- DNA ligaz nükleotitler arası bağı kurar.
Başlıca DNA tamir mekanizmaları şunlardır:
- Doğrudan Tamir (Direct Repair): Mutajenler tarafından oluşturulan kovalent modifikasyonları özel enzimlerle tersine çevirir.
- Fotoliaz: UV ışınlarının oluşturduğu timin dimerlerini ayırır (insanlarda bulunmaz).
- Alkil Transferaz: Alkilleyici mutajenlerin eklediği metil/etil gruplarını uzaklaştırır.
- Baz Çıkarma Tamiri (Base Excision Repair – BER): DNA N-glikozilazlar, anormal bazları tanır, çıkarır ve apürinik/aprimidinik bölgeler oluşturur.
- Nükleotit Çıkarma Tamiri (Nucleotide Excision Repair – NER): Çeşitli DNA hasarlarını (timin dimerleri, tautomerik kaymalar) tanır ve hasarlı bölgeden 24-32 nükleotitlik bir parçayı çıkararak tamir eder.
- ⚠️ Hastalıklar: Xeroderma pigmentosum (XP), Cocayne Sendromu (CS) gibi hastalıklarda NER genlerindeki kusurlar görülür ve güneş ışığına aşırı hassasiyetle karakterizedir.
- Yanlış Eşleşme Tamiri (Mismatch Repair): Replikasyon sırasında oluşan yanlış baz eşleşmelerini düzeltir. Parental ipliği metilasyon işaretleri (örn. GATC dizileri) aracılığıyla tanır.
- ⚠️ Hastalıklar: Bu sistemdeki gen kusurları (örn. hMSH2, hMLH1 mutasyonları) kalıtsal nonpolipozis kolorektal kansere neden olabilir.
- Rekombinasyonel Tamir: Hasarlı DNA'nın hasarsız bir molekülle rekombinasyonu yoluyla lezyonları onarır (örn. timin dimerlerinin atlanması sonrası oluşan boşlukların doldurulması).
- Çift Zincir Kırıkları (Double Strand Break – DSB) Tamiri: DNA hasarlarının en tehlikelisidir.
- Homolog Rekombinasyon Tamiri (HRR): Diploid hücrelerde homolog kromozomların (S ve G2 evresinde kardeş kromatidlerin) kalıp olarak kullanıldığı, hatasız bir tamir yoludur.
- ⚠️ Hastalıklar: BRCA1 ve BRCA2 genlerindeki mutasyonlar meme kanseri ve Fankoni anemisi gelişimine neden olabilir.
- Nanhomolog Uç Birleştirme Tamiri (NHEJR): Kırık kromozom uçlarını doğrudan birleştirir. Hata sıklığı daha yüksektir ve parça kayıplarına neden olabilir.
- Homolog Rekombinasyon Tamiri (HRR): Diploid hücrelerde homolog kromozomların (S ve G2 evresinde kardeş kromatidlerin) kalıp olarak kullanıldığı, hatasız bir tamir yoludur.
- Hata Eğilimli (SOS) Tamir (Error-Prone Repair): Büyük DNA hasarları olduğunda alternatif polimerazlar (örn. Pol V) kullanarak replikasyonu sürdürür ancak yüksek hata oranına sahiptir.
- Transkripsiyon-Tamir-Eşlikçi-Faktör (TRCF): RNA polimerazın transkripsiyon sırasında bir lezyonla karşılaştığında, NER sistemindeki proteinleri hasarlı bölgeye yönlendirerek tamiri sağlar.
Sonuç
DNA'nın genetik materyal olarak karmaşık yapısı ve işlevleri, mutasyonların kaçınılmaz bir parçasıdır. Bu mutasyonlar, bir yandan evrimin ve tür içi çeşitliliğin temelini oluştururken, diğer yandan genetik hastalıkların ana nedenidir. Hücreler, genomik bütünlüğü korumak ve bu zararlı değişikliklerin etkilerini en aza indirmek için çok sayıda ve özelleşmiş DNA tamir mekanizması geliştirmiştir. Bu tamir sistemlerinin anlaşılması, genetik hastalıkların teşhis ve tedavisi için kritik öneme sahiptir.